Identifier des mécanismes de résistance pertinents pour les patients
Notre objectif principal est d’identifier des mécanismes de résistance cliniquement pertinents et utilisables, c’est-à-dire qui auront un impact réel sur la prise en charge des patients.
Pour cela, nous mettons en place des essais cliniques dédiés aux ADC, permettant de collecter des échantillons biologiques précieux issus de patients sensibles ou résistants à un ADC donné.
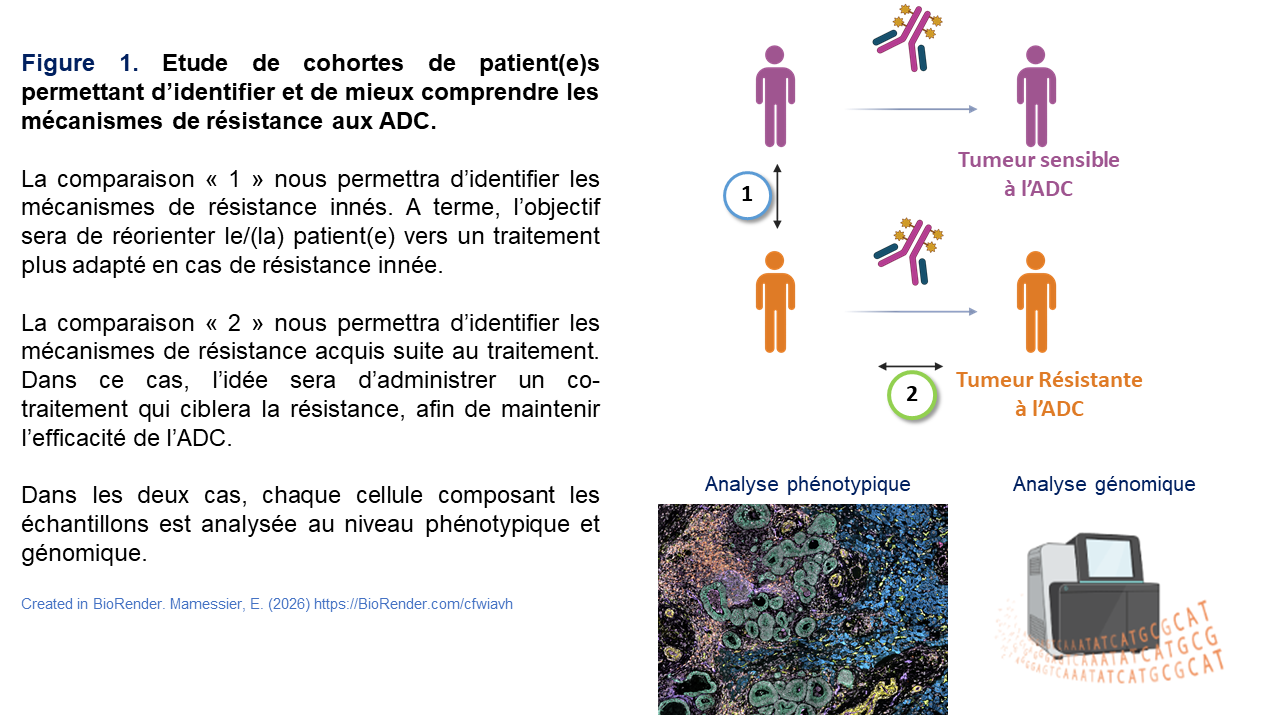
Nous réalisons ensuite des comparaisons systématiques (Figure 1) :
- soit entre groupes de patients avant traitement, comparaison « 1 »
- soit entre prélèvements séquentiels provenant d’un même patient au cours du temps, comparaison « 2 »
Ces analyses reposent sur des approches ultra-résolutives, souvent à l’échelle de la cellule unique, nécessitant le recours à des technologies innovantes, à la fois plus sensibles et plus précises, et parfois devant être adaptées aux contraintes des échantillons disponibles.
Ce niveau de résolution est indispensable pour révéler des mécanismes de résistance souvent multiples, discrets, profondément enfouis, et parfois situés là où on ne les attend pas.
Une fois identifiés, ces mécanismes de résistance peuvent jouer un double rôle :
- servir de biomarqueurs, permettant d’identifier précocement les patients à risque de développer une résistance ;
- constituer de nouvelles cibles thérapeutiques, à associer aux ADC afin de maintenir la sensibilité au traitement le plus longtemps possible.
Pour atteindre cet objectif, nous développons également des outils et des modèles d’étude directement transférables vers la pratique clinique.
________________________________________
Anticiper la résistance pour mieux la traiter
Cet axe de recherche vise à valider l’utilisation de marqueurs prédictifs de réponse aux ADC, identifiés grâce aux approches précédentes. L’objectif est de déterminer, avant l’administration du traitement, si un patient est susceptible de répondre à l’ADC qui lui est proposé.
Pour cela, nous avons là encore besoin de travailler à partir d’échantillons issus de cohortes locales et de bases de données existantes.
Deux situations peuvent se présenter :
- Le marqueur de résistance est présent avant traitement,
Dans ce cas, nous développons des outils de détection utilisables en routine clinique. En cas de positivité, des signatures de réponse à d’autres traitements sont évaluées afin de proposer une stratégie thérapeutique alternative plus adaptée.
- Le marqueur de résistance apparaît au cours du traitement,
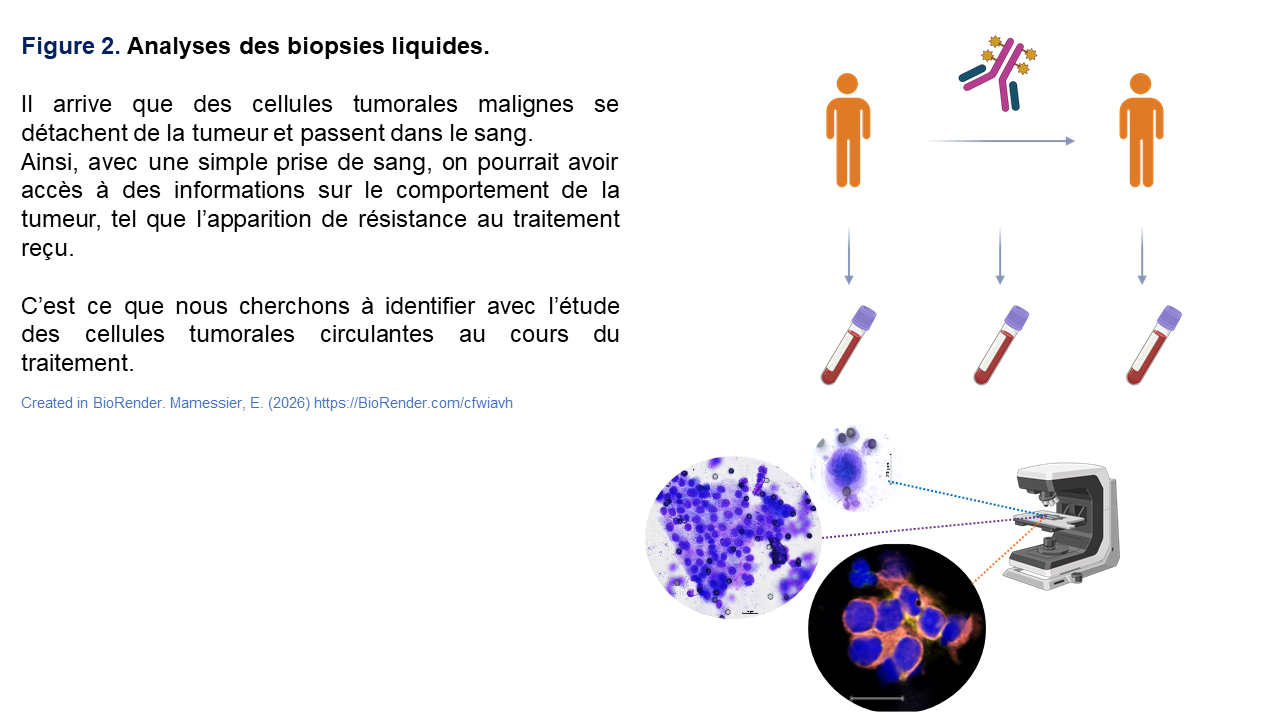
Il devient alors crucial de le détecter le plus précocement possible afin d’intervenir rapidement. Pour cela, nous utilisons des analyses à partir de prélèvements sanguins, ou biopsies liquides, qui présentent l’avantage majeur d’être peu invasives, répétables et réalisables dans de nombreux contextes cliniques (Figure 2).
________________________________________
Traiter la résistance lorsqu’elle est installée
Ce second axe de travail a pour objectif de contrecarrer la résistance aux traitements lorsqu’elle est déjà présente. Pour cela, nous utilisons des modèles expérimentaux permettant de tester et d’anticiper l’efficacité des associations thérapeutiques.
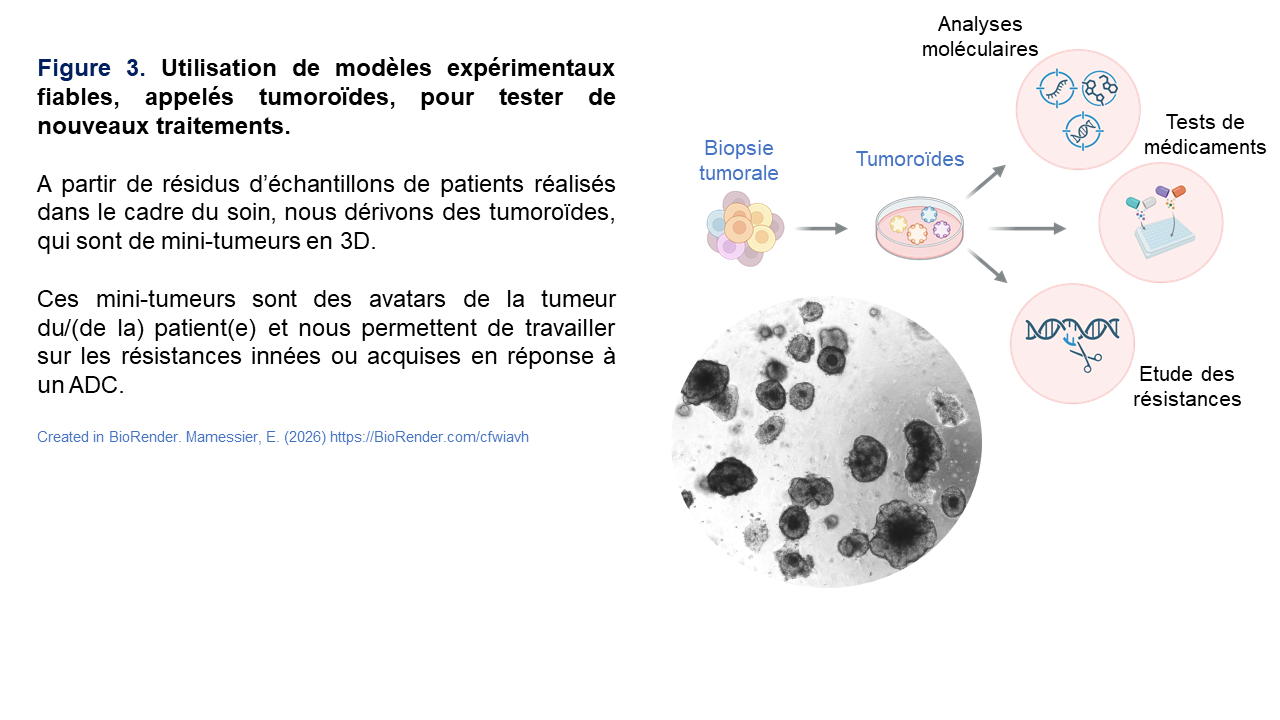
Nous travaillons notamment avec des tumoroïdes, des mini-tumeurs tridimensionnelles (Figure 3) dérivées directement d’échantillons de patients et conservant les caractéristiques biologiques de la tumeur d’origine.
Ces modèles particulièrement pertinents, pouvant être associés à des technologies de modification génétique telles que CRISPR, permettent de reproduire ou d’induire des mécanismes de résistance et de tester différentes combinaisons de traitements dans une logique quasi personnalisée.
Conclusions :
Notre équipe a à cœur de développer ses projets de recherche directement à partir des problématiques rencontrées dans la pratique clinique. Nous pensons que c’est ainsi que nous serons le plus utiles pour faire reculer la résistance aux traitements et de façon plus globale, la progression tumorale.
Définitions
Biopsie liquide : analyse de cellules ou de fragments tumoraux à partir d’une simple prise de sang.
Tumoroïdes : mini-tumeurs en 3D, créées en laboratoire à partir d’une biopsie tumorale.
CRISPR : technologie qui permet de modifier très précisément l’ADN d’un organisme vivant — comme une paire de ciseaux moléculaires programmables.